细胞动力学研究新进展:细胞定向迁移调控分子动力学机制及其功能的结构基础解析
- 时间:2013-06-19 06:19:25 来源:中国科大新闻中心|http://news.ustc.edu.cn/
近日,中国科大暨安徽细胞动力学与化学生物学省级实验室细胞迁移与肿瘤转移动力学科研团队,利用功能蛋白质组学、结构生物学及纳米尺度分子成像技术,鉴定了GTP酶激活蛋白ACAP4调控细胞膜动力学的结构基础,并深入解析了细胞外微环境调控肿瘤细胞定向运动的分子动力学机制。6月17日,国际著名学术期刊《美国科学院院报》(Proceedings of the National Academy of Sciences of the United States of America)在线发表了这一成果。
细胞是生命活动的基本单元,细胞动力学与可塑性是决定个体发育与健康的物质基础与保证。细胞动力学与可塑性在分子水平上主要表现为蛋白质复合物在各种复杂层次和体系的作用模式与时空动态变化。该实验室在解析细胞迁移动力学与可塑性调控蛋白质网络分子机制时,利用功能蛋白质组学技术发现了一个新的ARF6 GTP酶激活蛋白ACAP4及其作用网络(Fang et al., Mol. Cell Proteomics. 2006; Ding et al., JBC. 2010; Yu et al., JBC. 2011)。ACAP4是一个特异性的ARF6激活蛋白,它通过促进GTP水解来调节ARF6在囊泡运输中的功能及其与细胞质膜作用,从而调控细胞迁移的动力学特征,但是人们对ACAP4调控细胞质膜可塑性的分子机制与结构基础仍然知之甚少。
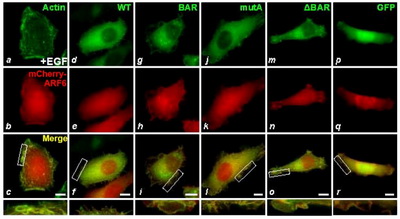 该研究团队最新研究揭示: ACAP4蛋白含有一个特异的BAR(Bin, Amphiphysin, and RSV161/167)结构域,表皮生长因子通过磷酸化BAR结构域中第34位酪氨酸、促进了ACAP4蛋白与细胞膜的结合,从而调控ARF6GTP/GDP循环的时空动力学特征,确定细胞迁移的方向性。该研究为解析磷酸化修饰ACAP4蛋白在不同微环境中调控肿瘤细胞转移可塑性与动力学提供了新的线索。该工作首次揭示了BAR结构域酪氨酸磷酸化是细胞迁移的重要调控机制,为肿瘤细胞转移信号转导通路的研究与干预提供了契机。
该研究团队最新研究揭示: ACAP4蛋白含有一个特异的BAR(Bin, Amphiphysin, and RSV161/167)结构域,表皮生长因子通过磷酸化BAR结构域中第34位酪氨酸、促进了ACAP4蛋白与细胞膜的结合,从而调控ARF6GTP/GDP循环的时空动力学特征,确定细胞迁移的方向性。该研究为解析磷酸化修饰ACAP4蛋白在不同微环境中调控肿瘤细胞转移可塑性与动力学提供了新的线索。该工作首次揭示了BAR结构域酪氨酸磷酸化是细胞迁移的重要调控机制,为肿瘤细胞转移信号转导通路的研究与干预提供了契机。
该论文第一作者为合肥微尺度物质科学国家实验室博士后研究员赵玄女和王冬梅。本研究得到了施蕴渝教授实验室及滕脉坤教授实验室的大力支持。该项目获得科技部、教育部、中科院、国家自然科学基金委和安徽省科技厅等资助。
细胞是生命活动的基本单元,细胞动力学与可塑性是决定个体发育与健康的物质基础与保证。细胞动力学与可塑性在分子水平上主要表现为蛋白质复合物在各种复杂层次和体系的作用模式与时空动态变化。该实验室在解析细胞迁移动力学与可塑性调控蛋白质网络分子机制时,利用功能蛋白质组学技术发现了一个新的ARF6 GTP酶激活蛋白ACAP4及其作用网络(Fang et al., Mol. Cell Proteomics. 2006; Ding et al., JBC. 2010; Yu et al., JBC. 2011)。ACAP4是一个特异性的ARF6激活蛋白,它通过促进GTP水解来调节ARF6在囊泡运输中的功能及其与细胞质膜作用,从而调控细胞迁移的动力学特征,但是人们对ACAP4调控细胞质膜可塑性的分子机制与结构基础仍然知之甚少。

该论文第一作者为合肥微尺度物质科学国家实验室博士后研究员赵玄女和王冬梅。本研究得到了施蕴渝教授实验室及滕脉坤教授实验室的大力支持。该项目获得科技部、教育部、中科院、国家自然科学基金委和安徽省科技厅等资助。
相关文章
- 中国科大揭示层间拖拽耦合在远程莫尔调控中的应用2025-10-27 10:39:01
- 中国科大开发毫秒时间分辨冷冻电镜技术,破解神经突触传递生物物理机制2025-10-17 09:00:42
- “看清”单链DNA上每一个碱基的结构——中国科大算法辅助的针尖增强拉曼显微成像实现单碱基精度识别2025-10-16 15:16:49
- 中国科大发展“绿氢冶铁” 新技术2025-10-09 16:02:57
- 中国科大在一维极化子超晶格精密探测研究中取得重要进展2025-09-24 18:18:38
- 中国科大揭示二维笼目晶格中的电子手性可导致声子手性2025-09-22 09:02:40

