抗艾滋病药物研究取得新进展
- 时间:2005-03-26 01:19:00 来源:合肥微尺度物质科学国家实验室|http://www.hfnl.ustc.edu.cn
合肥微尺度物质科学国家实验室低维物理与化学研究部汪志勇教授课题组与美国西莱山医学院(Mount Sinai School of Medicine)合作, 以艾滋病毒转录共激活因子特定区域(PCAF/BRD)为基础进行抗艾滋病药物的研制,最近取得了重要进展。
众所周知,艾滋病是由人免疫缺陷病毒(HIV)引起的一种致命的传染病。自1981年在美国首次发现以来,已在全球迅速蔓延。近年来我国爱滋病患者人数也迅猛膨胀,且呈加速趋势,它的危害已引起各国政府的高度重视。
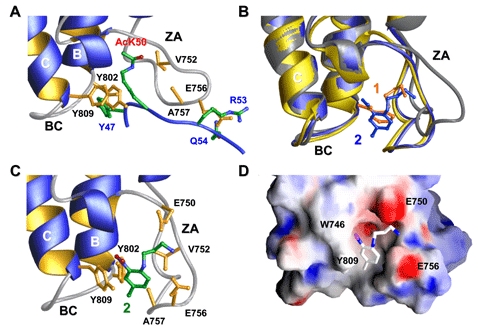 |
| 图1. PCAF BRD与配体相互识别的结构基础. (A) Tat-AcK50 蛋白与PCAF BRD的识别过程; (B) 游离的 BRD (灰色), 和化合物1(橙色)2(蓝色)复合的BRD; (C) BRD/2(绿色)复合物结构以及络合的部位; (D) 化合物2络合口袋示意图. |
艾滋病-1型病毒(HIV-1)的快速变异导致了治疗艾滋病药物研制的极大的困难。最近,汪志勇教授课题组与其合作伙伴——美国西莱山医学院的MingMing Zhou 教授领导的科研小组紧密合作、共同努力,以PCAF/BRD而不是病毒蛋白(HIV-Tat)为靶点来阻断艾滋病毒的基因表达, 研究表明HIV-1的转录并复制(被感染过程)需要艾滋病毒的反式转录蛋白(Tat)中乙酰化赖氨酸残基(AcK50)与人体核转录共激活因子(PCAF)之间独特的相互作用才能完成(图1)。在此基础上,他们设计并合成了一系列的小分子化合物。通过核磁共振检测技术已成功筛选出三个先导化合物[N1-(2-硝基-苯基)-1,3-丙二胺] (1)(IC50=5.1µm)、[N1-(2-硝基-4-甲基苯基)-1,3-丙二胺](2)(IC50=1.6µm) 和 [N1-(2-硝基-4-乙基苯基)-1,3-丙二胺] (3)(IC50=7.2µm)。这些先导化合物能够选择性地与PCAF/BRD结合,其结合的牢固程度大大超过了与艾滋病毒中的乙酰化反式转录蛋白(AcKTat)结合的强度。通过测定它们与PCAF/BRD形成的复合物三维结构, 发现它们与PCAF/BRD的结合方式类似于AcKTat与PCAF/BRD的结合方式,从而为艾滋病的治疗发现了潜在的新靶点,为无抗药性的治疗艾滋病药物的研制提供了新的途径。
该研究的初步结果发表在美国化学会志上(J. Am. Chem. Soc., 2005, 127, 2376),审稿人评价说:“所有的实验工作是高水平的,该项工作使得抗艾滋病药物新靶点的确认迈出了重要的一步”。目前该项合作研究正在深入开展过程中。
相关文章
- 中国科大开发毫秒时间分辨冷冻电镜技术,破解神经突触传递生物物理机制2025-10-17 09:00:42
- “看清”单链DNA上每一个碱基的结构——中国科大算法辅助的针尖增强拉曼显微成像实现单碱基精度识别2025-10-16 15:16:49
- 中国科大发展“绿氢冶铁” 新技术2025-10-09 16:02:57
- 中国科大在一维极化子超晶格精密探测研究中取得重要进展2025-09-24 18:18:38
- 中国科大揭示二维笼目晶格中的电子手性可导致声子手性2025-09-22 09:02:40
- 中国科大基于频率测量法实现超高精度分子线强度比2025-09-21 08:56:04

